Étiologie, classification, image clinique, diagnostic et traitement de la leucémie myéloïde aiguë.
Contenu
 Leucémie aiguë — Groupe hétérogène de clonal
Leucémie aiguë — Groupe hétérogène de clonalMaladies tumorales du tissu hématopoïétique caractérisée incontrôlée
prolifération, perturbation de la différenciation et de l'accumulation dans la moelle osseuse et
Sang périphérique de cellules hématopoïétiques immatures.
La leucémie aiguë est de 2-3% de tumeurs malignes
homme. L'incidence de la leucémie nette est en moyenne de 3 à 5 cas sur
100 000 habitants. Dans 75% des cas, la maladie est diagnostiquée chez les adultes, 25%
Cas — dans les enfants. Le ratio moyen de la leucémie tranchante myéloïde et lymphoïde
est 6: 1. Chez les patients adultes de plus de 40 ans de 80% des cas
présenté par des formes myéloïdes, chez les enfants — 80-90% — lymphoïde. Médian
Age Patients atteints de leucémie aiguë non limimencée — 60-65 ans, forte
leucémie lymphoblastique — 10 années.
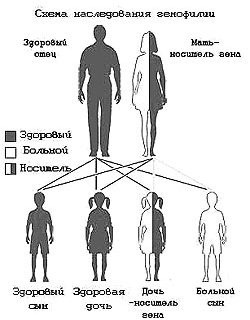
Il y a une probabilité génétique de développer une aiguë
Leucoza myéloïde. Il y a un grand nombre de rapports de cas familiaux
Maladies, la probabilité d'un IML pour les parents les plus proches du patient
trois ci-dessus. Un certain nombre d'états innés peuvent
augmenter la probabilité d'oml. Le plus souvent, il s'agit de syndrome de la probabilité d'un IML relevé dans
dix — 18 fois.
Certains cancérogènes
(provoquant des agents de tumeurs) peut être considéré comme des facteurs étiologiques
Oml, tels que l'essence, le tabac fumant et les rayonnements ionisants. Le plus important
Le facteur de risque est de plus de 65 ans.
L'influence de l'individu
Les caractéristiques génétiques du corps, ainsi que l'impact sur le corps d'exogène
Les facteurs se manifestant dans le développement de la leucémie myéloïde aiguë secondaire,
composants de 5-20% de tous les cas d'IML. En particulier, l'IML peut développer
Les personnes auparavant subissent un traitement avec divers modes de chimiothérapie
Autres formations malignes.
La présence de la phase précédente dans
la forme de syndrome myélodsplasique (MDS) le plus courant chez les personnes âgées
Les patients aussi sont un facteur de risque important OML. Antitugéniste
Effets chimiothérapeutiques, en particulier médicaments en alkylation, anthraciklines
et les épipodophillexines, augmente la probabilité du développement du secondaire
Oml / secondaire MDS. La probabilité la plus élevée de la maladie tombe pendant 3-5 ans
Après la chimiothérapie. L'application combinée de la chimiothérapie / radiothérapie est également de manière significative
Augmente le risque de MDS IML / secondaire secondaire. Il convient de noter que secondaire
Leucémie / MDS ne surgissent pas chez tous les patients recevant antitumoral
traitement.
La leucémie aiguë est
Par conséquent endommager — Mutations — Dans le matériau génétique du clone
Cellule de cerceau. En conséquence, le niveau moléculaire se produit
Événements menant à une violation du contrôle sur le cycle cellulaire, change
Processus de transcription et produits d'un certain nombre de protéines clés-régulateurs. Malin
Les méloblastes font progresser les cellules avec oml,
incapable de maturation et de différenciation à la suite d'une faculté altérée
Contrôle génétique et accumulation
dans la moelle osseuse. Cellules Lakeclone
interférer avec les activités des cellules normales, les poussant de la moelle osseuse.
Actuellement tous tranchants
La leucémie est prise pour se diviser sur la leucémie myéloïde et lymphoblastique aiguë.
La classification de la leucémie myéloïde Sharp est présentée ci-dessous.
Classification de la leucémie myéloïde tranchante
| Prénom Sous-espèces | La description |
|
Oml S Changements génétiques caractéristiques |
Chez des patients présentant une telle sous-espèce de l'IML Des niveaux de rémission généralement élevés et les prévisions sont mieux relativement avec l'OML des autres sous-espèces. |
|
Oml avec dysplasie Plusieurs Rostkov |
Cette sous-espèce Comprend les patients atteints de syndrome de myelodsplastic précédent (MDS) ou maladie myéloproliférative (MPB), qui va à l'iml. Cette sous-espèce de l'IML est plus fréquente chez les personnes âgées et Diffère des perspectives défavorables. |
|
Oml i MDS associé au traitement précédent |
Cette sous-espèce OML inclut les patients recevant la chimie et / ou le traitement des radiations après qui est venu l'iml ou le MDS. Avec ces leucémies, il peut y avoir des caractéristiques Changements de chromosomes, les prévisions pour eux sont souvent pires. |
|
Oml, N Sous réserve des signes de sous-espèces énumérées |
Inclut Sous-espèces OML qui ne sont pas incluses dans celles énumérées ci-dessus. |
Franco-américain-britannique
classification
Classification Franco-American-Britannique (Fab)
Le système partage un IML à 8 sous-espèces, de M0 de M7, sur la base des types
cellules — prédécesseurs de leucocytes et sur le degré de maturité du changement
cellules. La détermination des cellules malignes est effectuée sur la base
signes externes avec microscopie légère et / ou cytogénétiquement, détectant
Déviations sous-jacentes des changements de chromosomes. Différentes sous-espèces de l'IML
Prévisions et réponse différentes au traitement. Malgré les avantages de la classification de l'OMS,
Le système Fab est toujours largement utilisé. Par fab il y a huit sous-types
Oml.
| Sous-espèces | Nom | Changements citogénétiques |
| M0 |
Minimalement différencié Leucémie myéloblastique aiguë |
|
| M1 |
Épicé Leucémie myéloblastique sans maturation |
|
| M2 |
Épicé Leucémie myéloblastique avec maturation de granulocytes |
T (8; 21) (Q22; Q22), T (6; 9) |
| M3 |
Promelocyrtar, Ou concours aigu Leucémie (plancher OP) |
T (15; 17) |
| M4 | Épicé Leucémie myélomocytaire |
INV (16) (P13Q22), Del (16q) |
| M4eo |
Myélonocital Combiné à l'éosinophilie de la moelle osseuse |
Inv (16), T (16; 16) |
| M5 |
Monoblastique aigu leucémie (m5a) ou aiguë Leucémie monocystataire (M5B) (M5B) |
Del (11q), T (9; 11), t (11; 19) |
| M6 |
Érythitoïde épicé leucémie, y compris la leucémie érythrocytaire (M6a) et très rare propre Leucémie érythoïde (M6B) |
|
| M7 |
Épicé Leucémie mégakaryoblastique |
T (1; 22) |
| M8 |
Basophile aigu leucémie |
Image clinique
L'image clinique de la leucémie aiguë est déterminée par gravité
Syndromes de base:
-
Anémique — niveaux d'hémoglobine réduits et
le nombre d'érythrocytes, qui se manifeste
faiblesse, diminution de la capacité de travail, somnolence, manifestations
Insuffisance cardiaque, battement de coeur,
faiblesse, essoufflement, pâleur de peau et de muqueuses, orthostatique
hypotension, angine secondaire et infarctus du myocarde, intelligent
Chromota, clinique d'insuffisance respiratoire chez les patients chroniques
Maladies broncho-pulmonaires (MPOC). -
Granulocyteopénique — Complications infectieuses,
En raison d'une diminution du nombre de granulocytes dans le sang, qui se manifeste par une température élevée et une intoxication, ainsi que
Clinique locale (districts nécrotiques, stomatite ulcéreuse, ostéomyélite
Mâchoires après l'extraction de la dent) ou généralisée (sepsis, endocardite infectieuse),
plus souvent bactérienne, infection. -
Hémorragique
— Hémorragie dans la peau et les mucous, nasal et gum saignant,
Saignements gastro-intestinaux et rénaux, saignements utérins, élevés
Fraction de sang pendant les interventions opérationnelles. -
Proliférateur
— Lymphadénopathie, splénomégalie, hépatomégalie, gingivite hyperplastique,
Douleurs dans les os, troubles de la fonction des nerfs cérébraux crâniens, maux de tête, violations
Vision, générale et focale neurologique
Symptomatics, maux de tête, priapisme. -
Indexication
— Faiblesse, déclin de l'appétit, perte de poids, transpiration.
Diagnostic de la leucémie nette
 Première
Première
L'étape dans le diagnostic est
Analyse clinique du sang en prenant des échantillons de sang des veines. Dans l'échantillon de sang
Le nombre de cellules sanguines (érythrocytes, leucocytes et leurs sous-types est déterminé et
Aussi des plaquettes). Quand la découverte d'une analyse clinique du sang plus de 20%
Les cellules de souffle peuvent être diagnostiquées avec de la leucémie aiguë.- À
l'absence de sang suffisant pour diagnostiquer le nombre de coups, ainsi que
Le but de la vérification précise du diagnostic en utilisant des méthodes supplémentaires
Des études sont prises pour mener une biopsie d'aspiration de la moelle osseuse.
L'étude de la moelle osseuse comprend une étude d'aspiration de la moelle osseuse
(Analyse de mon examen cytologique cellogramique), dans de rares cas, la dépilobiopsie est effectuée
moelle osseuse pour une étude histologique de la moelle osseuse. - DANS
Qualité des méthodes de recherche supplémentaires pour déterminer la variante de la pointe
La leucémie et les marqueurs pronostiques sont effectués:
-
Cytoochimique
Recherche (myeloperixidase, eSerase, glycogène) -
Cytogénétique
étudier — détection d'anomalies chromosomiques, telles que l'absence ou
Chromosomes supplémentaires dans les cellules de la moelle osseuse par analyse standard
Métafaz ou méthode de poisson
(Fluorescent
In. Hybridation
Situé — Méthode basée sur la capacité
ADN chromosomique (cible) à contacter sous certaines conditions avec petit
Séquences d'ADN (sondes), complémentaire de cet ADN chromosomique. À
L'adhésion à la sonde de substance fluorescente produisit une analyse de l'ADN par son
Emplacement des cellules dans les cellules d'interfase). Les résultats de cytogénétique
Des études sont portées à la fois de l'importance du diagnostic et du pronostic.
| Exode | Déviation | Survival de 5 ans | Fréquence de récupération |
| Favorable |
T (8; 21), T (15; 17), INV (16) |
70% | 33% |
| Satisfaisant |
Pas Révélé, +8, +21, +22, del (7q), del (9q), violations 11q23, tous les autres Changements structurels ou numériques |
48% | cinquante % |
-
Biologique moléculaire
recherche (recherche génétique est effectuée pour identifier la caractéristique
mutations pouvant affecter l'issue de la maladie — Par exemple, FLT3-Tyrosine Kinase, Gene CD117, a pris sa retraite pour la synthèse du récepteur
Facteur de croissance des cellules souches, Genes Cebra,
BAALC, ERG, NPM1. -
Étudier
Sur les cellules tumorales des antigènes différentiels (CD) par cytométrie de flux (immunophénotypage).
Dans l'avenir chez les patients avec forte
Études de la leucémie sur la moelle osseuse afin de
Déterminer l'effet de la thérapie, l'exhaustivité de la rémission obtenue et la phase de processus
(rémission, stabilisation, progression).
Étapes et phases cliniques de la maladie
-
Primaire actif
étape — Intervalle de temps entre les premières manifestations cliniques
Maladies, diagnostic et première rémission complète -
Plein
Remission hématologique clinique — Le nombre de cellules de souffle dans le myélogramme
Diminue moins de 5%, il n'y a pas de foyers leucémiques extrêmement visa
Les lésions, tandis que dans le sang périphérique ne devraient pas être des cellules de souffle,
Nombre de plaquettes 100×109 / L leucocytes 2.5 x
109 / L, Granulocytes 1.0 x
109 / L, niveau de l'hémoglobine de 100 g / l.
Récemment, le concept de biologie cytogénétique et moléculaire
remise. -
Étape
maladie minimale résiduelle (résiduelle). -
Recourber
Maladies (moelle osseuse, surtension extraotique). -
Terminal
étape.
Traitement
Avant de commencer le traitement, une clinique complète
Examen des patients pour évaluer l'état de pathologie concomitante
Systèmes cardiovasculaires, respiratoires, urogénitaux, système nerveux central.
Il comprend un test sanguin biochimique complet, un coagulogramme, un examen sur
Hépatite B et C, VIH, virus du groupe Herpes. Ultrasound d'organes
Cavité abdominale, Étude de la radiographie de la poitrine / ordinateur
Tomographie de la poitrine, la cardiographie ECG / ECHO, CT / IRM Head, Inspection
neurologue, oculiste et t.RÉ. Tout cela est nécessaire pour le bon choix de traitement et
Prévenir les complications.
Méthodes de traitement
Les patients atteints d'IML dépendent du type de maladie, de facteurs pronostiques, de l'âge
le patient, ainsi que la pathologie connexe et peut être divisé en
Méthodes thérapeutiques potentiellement guérisantes et traitement de soutien.
Soutenir I
Thérapie symptomatique
Fondation
Le traitement de l'OML est une thérapie de soutien, qui comprend le traitement des infections intercurrentes, de l'état substantiel
diathèse, traitement de remplacement avec composants sanguins, ainsi que traitement
Pathologie concomitante.
Basé sur
La thérapie de soutien des patients atteints de MDS est une thérapie de remplacement
Composants sanguins. Les patients ayant un faible risque de développement oml anémie peuvent être
Clinique principale problème significatif. Thérapie de remplacement
facilite les symptômes de l'anémie et, par conséquent, est un traitement important.
La fréquence
Les transfusions dépendent de l'état du patient, de la gravité de l'anémie, ainsi que de
Pathologie concomitante, en particulier le besoin de composants débordants
sang lors du développement des saignements patients. Le résultat de la thérapie de substitution
est une augmentation du niveau d'hémoglobine, quelles études montrent,
a une corrélation positive avec un indicateur de qualité de qualité.
Transfusion
La masse plaquettaire est effectuée dans des cas où le nombre de plaquettes
extrêmement faible et / ou il y a des saignements dangereux. En développement
La coagulopathie (violations dans le système de coagulation de sang, par exemple la réduction de niveau
Fibrinogènes ou facteurs complexes de la prothrombine) Remplacement de la conduite
Thérapie des composants plasmatiques sanguins ou
Prépartes recombinantes (Novosvlen, Promromboplex et PR.)
Méthodes thérapeutiques potentiellement guérisantes
-
 Pour contrôler les symptômes de la maladie ou de la guérison de l'IML chez les jeunes patients, utilisez
Pour contrôler les symptômes de la maladie ou de la guérison de l'IML chez les jeunes patients, utilisez
Chimiothérapie intensive pour détruire le clone de pathologique
cellules et atteindre une longue rémission. Cette méthode de traitement a
Effets secondaires importants, tels que la perte de cheveux, l'apparition de la stomatite
cavité buccale, nausée, vomissements, apparence de tabouret liquide. En plus de ces côtés
phénomènes, chimiothérapie a des effets indésirables et sains
cellules qui nécessitent un long séjour en hématologique
Départements. À ce moment-là, le patient est effectué sur le sang sur le sang et
La masse thrombocyte, les médicaments antibactériens sont prescrits au combat
infection. Si la chimiothérapie à induction fournit un contrôle adéquat sur
cellules pathologiques (état de rémission), puis restauration de la normale
Les globules doivent commencer dans quelques semaines. Cependant, même dans les cas
Une maladie de traitement réussie peut être retournée — se reproduire. - Le seul
Procédé de traitement connu capable de guérir la plupart des patients atteints d'OML,
est la transplantation d'une tige hématopoïétique allogénique (donneuse)
cellules. Il convient de garder à l'esprit qu'il s'agit d'une procédure complexe liée aux risques
Complications tôt et tardives. Le résultat du traitement dépend du degré de compatibilité (compatibilité HLA) du donateur et du patient
(destinataire), ainsi que sur la disponibilité de cellules donneuses appropriées (disponibilité
Frères et / ou soeurs de sang compatibles, disponibilité de la banque donatrice). Ainsi
La façon dont il y a des témoignages stricts et des contre-indications pour ce type de traitement:
Il convient aux cas où les patients sont capables de transférer
Transplantation de cellules souches et a un donateur approprié et répondit un traitement chimiothérapeutique. - Étudier
Les mécanismes de développement de MDS / Secondaire IML, entrepris ces dernières années montraient,
que pour cette pathologie se caractérise par l'hypermétallisation de la région du promoteur
certains gènes-oncosupresseurs, qui mènent à «Silence» Ces gènes I
Prolifération des cellules tumorales et des transformations dans l'IML. Sur la base de ces connaissances
Les agents dits hypométalistes qui contribuent ont été développés
ADN hypothylation, provoquant l'expression plus tôt «Désactivée» Genov.
En mai 2004, Gestion
États-Unis de la lutte contre la nourriture et la drogue (alimentation et drogue administration, FDA) délivré la permission d'utiliser
Préparation par injection Azacytidin (Vaijaza) pour le traitement de tous les types de MDS. Dans la Fédération de Russie
Le médicament a été approuvé pour une utilisation en 2010, y compris pour le traitement de MDS et IML. Les résultats de l'étude ont montré que
Azacytidin prolonge de manière fiable la vie aux patients atteints de leucémie myéloïde aiguë,
Transplantation de cellules souches programmées / intensive
chimiothérapie. Les études montrent que le taux de survie des patients présentant une OML sans traitement moderne est de 1,6
mois, tandis qu'Azacytidin augmente la durée de vie avec IML
11,1 mois, possédant favorable
Profil de sécurité. outre,
le médicament, avec des qualifications suffisantes de personnel médical, peut
Appliquer Ambulateur.
Selon les protocoles adoptés en Russie, le traitement des patients IML, qui ne sont pas
Convient pour intensif
La chimiothérapie et l'OML secondaire sont effectuées par de faibles doses de cytarabine et / ou avec
en utilisant une thérapie de soutien [un]. Telle thérapie
Améliore la qualité de la vie des patients, mais n'augmente pas leur vie
En comparaison avec le cours naturel de la maladie. Tout usage
L'azacitidine dans cette catégorie de patients peut changer radicalement le flux
Maladies (tableau 1).
tableau
un. La survie totale moyenne chez les patients de l'IML, en fonction de la thérapie (indirecte
Données comparatives).
| Sans traitement | Thérapie de soutien | Doses faibles de cytarabine | Azacytidin | |
|
Oml, y compris numéro Oml S Le nombre d'explosions en myélogramme 20-30% |
1,6 | 13,4 | 17.0 | 24.5 |
Survie médiane des patients atteints d'OML (20-30% des explosions),
recevoir Azacytidine, augmente à 24,5 mois. Dans le même temps, les différences dans le groupe
Azacytidine avec des groupes de thérapie soutenante et de basses doses de cytarabine
statistiquement fiable (p = 0,045), quel que soit l'âge ou le caryotype, et
Les mois de vie facultatifs sont respectivement de 11,1 et 7,5 (médiane
La survie dans le groupe de thérapie de soutien est égale à 13.4 et dans le groupe bas
Doses de cytarabine — 17,0 mois) (analyse de la recherche de données III Phase AZA-001) [2]. Après 2 ans, 50,8% des patients du groupe étaient vivants
Azacitidine, qui est 2 fois plus que des groupes de comparaison (26,2%). Pour
Comparaison — Les patients présentant un OML qui ne reçoivent pas de thérapie moderne (naturel
Le cours de la maladie) meurt dans les 7 semaines du diagnostic.
 Pour les patients avec un IML, pas
Pour les patients avec un IML, pas
Chimiothérapie intensive / transplantation de cellules souches, traitement
L'azacytidine peut être le seul moyen de la vie prolongeant et
aider à atteindre une longue rémission. Dans l'étude AZA-001 dans le groupe Azacitidine à la réponse en thérapie
(Critères IWG
2000) a atteint 29% des patients (réponse complète et partielle), 49% — réalisé
Amélioration hématologique. Différences avec les groupes de comparaison («Attentif
thérapie», «Doses faibles de cytarabine») Statistiquement fiable (5 et 12%, 31 et 25%
respectivement). Le temps à la progression de la maladie était de 14,1 mois
Grouper «Azacytidididine» et 8,8 mois en groupes de comparaison (p = 0,047). Durée
La réponse hématologique était de 13,6 mois sur l'azacytidine par rapport à
5,2 mois sur la thérapie traditionnellement utilisée (p = 0,002).
Chez les patients atteints de MDS et IML qui ont reçu
La thérapie ascicitidine a été observée une probabilité d'indépendance plus élevée de
Transfusions de la masse d'érythrocyte: 45% des patients sont devenus indépendants de
Hémotransphe, tandis que sur les modes traditionnels — Seulement 11% (p < 0.0001).
Ainsi, le traitement de l'ascitidine des patients OML (20-30% des explosions)
accompagné non seulement par une espérance de vie plus élevée et un total
Fréquence de déclaration par rapport à la thérapie de soutien et aux basses doses de cytarabina,
mais aussi une amélioration et une indépendance hématologique plus élevées
Transfusions. Patients avec thérapie azacytidine à haut risque MDS
accompagné d'une augmentation du temps avant la transformation en une OML (17,8 mois contre 11,5 mois, p<0,001).
Azacytidin est inclus dans les protocoles internationaux de traitement
Les patients atteints de syndrome myélodsplasique et IML chez les patients de plus de 60 ans.
USA: Dans le Guide national de traitement de l'OML
Réseau oncologique (nationale Cancer Complet Réseau, NCCN, ETATS-UNIS) (2010) Azacytidine est recommandé pour l'application
Patients âgés de plus de 60 ans qui ne sont pas des candidats très visibles
Chimiothérapie. Les recommandations sont données avec un niveau de preuve élevé.
À
phénomènes indésirables de 3 à 4 degrés se développant dans le contexte du traitement de l'azacytidine,
Traiter hématologique (71.4%), y compris la thrombocytopénie (85%), la neutropénie
(91%) et anémie (5